

2月7日凌晨,华南农业大学发布消息称,发现穿山甲为新冠病毒潜在中间宿主。而此前,科研人员已经将新冠病毒的可能性源头锁定蝙蝠。
人类应当清楚,我们从来都不是地球的主人。可笑的是,作为地球生态这个古老循环中最年轻的一部分,我们却越来越容易忘记这一点。
而且,人类文明的快速发展让我们变得更易骄傲自大,更加坚信人类与那些被我们视为“野味”的野生动物是多么的不同。俗话说,万物守恒,因果相伴,在被人类肆意捕食、杀戮之时,野生动物也在以疫病为武器,向人类发起一场场复仇。
暗夜杀手:蝙蝠
蝙蝠这种动物生来就自带百余种病毒,它们本来很少有机会直接将病毒传染给人类。然而,一碗碗蝙蝠汤,一桌桌“蝠”寿宴,人类把这些原本离自己很远的病毒吃进了体内……
埃博拉出血热
埃博拉病毒,全名埃博拉出血热,是当代社会威胁人类健康的头号杀手。
作为一种烈性传染病,埃博拉出血热是人畜共患性传染病,对灵长类动物的杀伤力极大,其生物安全等级高达4级,是连艾滋病毒(3级)和 SARS 病毒(3级)都甘拜下风的病毒。目前,埃博拉病毒被世界公认为是可用作生物恐怖主义的工具之一。
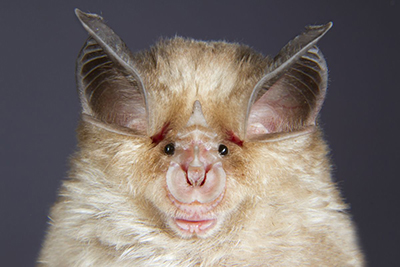
▲科学研究表明,蝙蝠是很多人畜共患病毒的宿主(图片来自网络)
从 1976 年“突袭”埃博拉河岸 55 个村庄开始,埃博拉病毒一度横扫非洲。在 2013 年世界卫生组织(WHO)官方通报的 24 起埃博拉疫情中,共有 2387 例确诊患者,死亡 1590 例。此后 WHO更是为此两度拉响国际公共卫生紧急事件(PHEIC)警报:2013-2016年,西非爆发全球最大规模的埃博拉疫情,造成28646人感染,1323 人丧生;2017 年疫情在刚果(金)卷土重来,截至 2019 年4月感染患者 1100 例,死亡患者 690 例……可以说,埃博拉出血热之于现代社会,恰如黑死病之于中世纪欧洲致死率均值可达50%,最高甚至能攀升至90%,是当今世界最为致命的病毒性出血热。
截至目前,科学界内尚不能完全确定埃博拉病毒的天然宿主,但学者普遍认为果蝠是这一病毒的真正元凶。1996 年研究人员在研究中发现,24 种植物及 19 种脊椎动物中,只有蝙蝠会受埃博拉病毒感染而自身不发病这是鉴别病毒天然宿主的重要特点之一。
期间,虽然人们也曾在大猩猩和黑猩猩的尸体中发现埃博拉病毒的基因片段,但鉴于该病毒对灵长动物的致死率极高,这与病毒天然宿主的理论并不相符,因而基本排除了猩猩等灵长类动物是宿主的可能。此后多年,越来越多的研究结果都将埃博拉病毒的真正宿主指向了果蝠。
值得注意的是,人类食用、与被感染的动物或尸体直接接触,都能传染埃博拉病毒:大猩猩等野生动物在食用了被果蝠啃咬后的果实后,自身即会被埃博拉病毒传染;当地人在食用了“丛林肉”(大猩猩、羚羊等野味)后被病毒传染,而后唾液和飞沫则进一步导致病毒的人际传播。
严重急性呼吸道综合征(SARS)
SARS,全称严重急性呼吸道综合征,是一种由冠状病毒所引发的全球性严重传染病。从 2002年 12 月首次被发现到 2003 年 7 月疫情基本结束,SARS 患者全球共计确诊 8069 例,死亡 774 例,仅中国地区确诊病例就高达7083例,死亡患者647例。

▲果子狸被科学家证实是将蝙蝠身上的SARS病毒传播到人身上(图片来自网络)
据 2004 年不完全统计,在 SARS 疫情最严重时期,该病致死率被认为介于 7%-15%,65 岁以上人群的死亡率更是高达 55%。受此次疫情影响,中国国民经济当年直接经济损失高达 933 亿元人民币。
起初,人们普遍认为果子狸是SARS病毒的宿主,但中国科学院武汉病毒研究所于 2013 年发表论文证实,中华菊头蝠才是 SARS 病毒的真正源头,果子狸作为中间宿主,是在被中华菊头蝠感染了病毒之后,间接将这一病毒传染给了人类。
中东呼吸综合征(MERS)
MERS,全称中东呼吸综合征,又是一场蝙蝠借由其它野生动物之手对人类的一次虐杀,只是这一次中间宿主由果子狸变为了骆驼。
2012 年,首例感染 MERS 病毒的患者在沙特阿拉伯被确诊。早期,因患者的临床症状与 SARS 病毒的临床症状颇为相似,MERS 病毒因而得名“类SARS 病毒”,是人类已知的第六种冠状病毒。
▲中东呼吸综合征是一场蝙蝠借由其它野生动物之手对人类的一次虐杀,只是这一次中间宿主由果子狸变为了骆驼(图片来自网络)
从 2012 年 9 月首次被发现到 2014 年 4 月,全球有 92 人因感染 MERS 病毒丧生,在此期间MERS 致死率高达 53%。2015 年 5 月,韩国首例MERS 确诊患者被发现,而后 MERS 病毒又引发了一场大规模的恐慌。截至 2015 年 7 月疫情基本结束,韩国因 MERS 被隔离人员共超过 1 万 6 千余人,确诊 186 例,死亡 36 例。此后几年 MERS 病毒时隐时现,截至 2019 年 11 月,全球 MERS 确诊病患已达 2494 例,死亡 858 例,平均致死率达 34.3%,
沙特阿拉伯地区是 MERS 的集中爆发地。最初,骆驼被认为是 MERS 病毒的真凶,然而经科学家最终确认,埃及墓蝠才是 MERS 病毒真正的宿主,因为人类接触或食用了被病毒感染的骆驼,间接受到了 MERS 病毒的入侵。
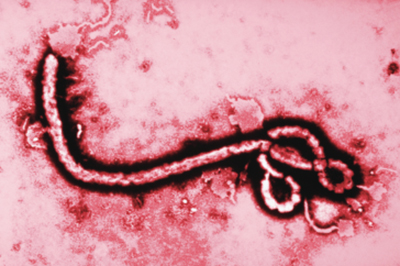
▲一个埃博拉病毒粒子拥有显著的“牧羊人的曲杖”结构。这是埃博拉病毒最早的照片之一,拍摄 于 1976 年10 月 13 日,拍摄者是当时在疾病控制中心工作的弗雷德里克·A·墨菲。神秘的结构性蛋白质像
绳索般缠在一起, 围绕着含有遗传密码的RNA单链。放大倍率:112000
千年恶魔·鼠
在传播疫病方面,啮齿类动物从来不弱于蝙蝠。试问冷兵器时代谁能做到“一日屠城”?答案就是鼠类。
一方面,人类快速扩张的城镇不仅蚕食了鼠类原本的家园,同时也迫使生存能力顽强的鼠类适应与人为伍,为它们将疾病传染给人提供了温床;另一方面,人类自古就不乏猎奇者,将各种野生鼠类搬上餐桌的所谓“老饕们”,在无形中又将人类往灾难面前推近了一步。
黑死病
作为人类最严重的瘟疫之一,黑死病是由鼠疫耶尔森菌感染引起的烈性自然疫源传染病,野生啮齿类动物诸如土拨鼠、旱獭是其主要宿主。中世纪时期,由于该疫病的传染性极强、致死率极高,且患者感染后会出现皮下出血变黑的症状,故而有“黑死病”之称。
在肆虐人类社会的百年时间里,黑死病在全球范围内消灭了近 7500 万人口,甚至间接影响了欧洲资本主义、乃至人类社会的发展进程⸺ 黑死病的频繁发生导致欧洲总人口锐减了 30%-60%。

▲画家笔下的黑死病“屠城”的末日景象(图片来自网络)
事实上,早在欧洲黑死病大爆发之前,拜占庭帝国曾在公元 541-542 年爆发过一次大规模的鼠疫(查士丁尼瘟疫),导致君士坦丁堡近40%的居民、东罗马帝国 25% 的总人口丧生。由于此次鼠疫来得快去得也快且没有复发,故而很快就被淹没在了历史长河。直至 1347 年 10 月,首例黑死病在西西里岛被发现,并用不到 4 个月就快速席卷整个意大利。两年时间里,匈牙利、波兰、普鲁士、苏格兰、俄国……越来越多的欧洲国家被波及,尸体堆积如山,四年时间欧洲一半人口因黑死病而丧生。
此后,欧洲又多次爆发了大规模的黑死病,1629-1631 年意大利、1665-1666 年伦敦、1679 年维也纳、1720-1722 年马赛、1771 年莫斯科……可以说,在发现抗生素之前,隔离城镇至最后一名疫患自行消亡,这种“听天由命”式的防疫方式几乎是人类对抗黑死病的唯一办法。
毋庸置疑,鼠类是黑死病的罪魁祸首:中世纪,由于气候及人类活动(如蒙古帝国的军事活动)影响,鼠类被迫从干旱的草原向人口密集的欧洲城镇“逃亡”,与鼠类一同迁徙而来的当然还有鼠疫杆菌。它们借助寄生于老鼠的跳蚤之“嘴”,在后者每一次看似漫不经心地叮咬中传播,轻而易举突破了人类社会彼时那道本就不堪一击的卫生防线,对人类大开杀戒。
猴天花
2018年英国科学家曾发出警告,提醒人类警惕一种“变种天花”
的卷土重来猴天花。
猴天花别称猴痘,与曾经肆虐全球的天花病毒是近亲,是一种人畜共患的传染性疾病,其中又以灵长类动物最易受到感染。不同于天花病毒,猴天花病毒的致死率最高只有 11%,但儿童多为易感人群,且病愈后患处皮肤会变为“麻子”。
在人类正式宣布消灭天花病毒之前 10 年的 1970 年,猴天花病毒首现于刚果(金)。此后,该病曾于 1996-1997 年在当地二度爆发。
2003 年,美国包括俄亥俄州、密苏里州等在内的 6 个州突然爆发猴天花疫情,一个月内共有 71 人确诊感染,但所幸并无人员死亡。后经调查发现,美国此次疫情罪魁祸首是一名患者家中新来的宠物⸺一只冈比亚鼠(草原土拨鼠)。
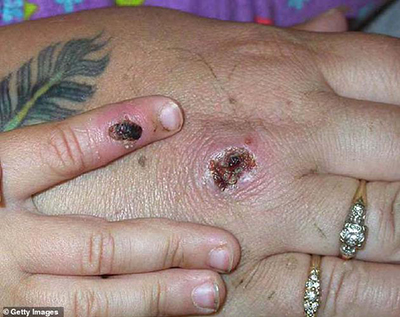
▲2003年出现第一例猴天花病毒案例,图中是患者的手(图片来自网络)
目前,人类尚无法准确认定猴天花病毒的真正自然宿主,但自2003 年至今,科学家们多次在松鼠、冈比亚鼠等啮齿类野生动物身上发现这一病毒,冈比亚鼠的嫌疑最重,被抓伤、咬伤、与受感染的宠物(如猫狗)直接接触都会致人类感染,空气和接触性传播均能加速病毒的人际传播。
斑疹伤寒
作为一种急性传染病,斑疹伤寒是鼠类带给人类的又一种疫病。总体来说,斑疹伤寒可分流行性斑疹伤寒和地方性斑疹伤寒,目前只有后者是被公认的自然疫源性疾病。
地方性斑疹伤寒由莫氏立克次体(RickettsiaMooseri)引起,因其主要宿主为鼠类,再由鼠虱传播给人类,故而又被称作蚤型斑疹伤寒或鼠型斑疹伤寒。
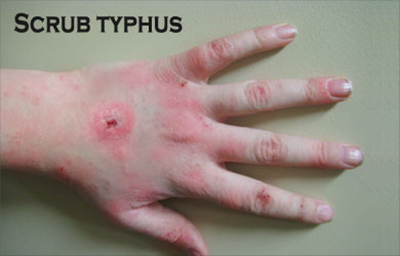
▲斑疹伤寒案例,图中是患者的手(图片来自网络)
作为一种全球性的疫病,斑疹伤寒至今每年感染的人数仍高达 100 万例,其中又尤以亚太不发达地区最受影响。尽管致死率不及黑死病,如果不采取及时的治疗措施,斑疹伤寒的致死率亦能达到70%,被感染的患者会出现持续高热、心律失常、狂躁恍惚等症状。
早在第二次世界大战期间,斑疹伤寒就曾肆虐缅甸和锡兰地区。美国军事家麦克阿瑟在回忆录中指出,在二战科科达小径战役中,因感染斑疹伤寒致死的人数与因武器受伤致死的人数比高达 5:1。与此同时,盟军在新几内亚战役和瓜达尔卡纳尔战役中也饱受斑疹伤寒的折磨。
拉沙热
与黑死病和斑疹伤寒不同,由拉沙病毒所引发的拉沙热疫病,无需通过鼠身上的寄生虫传播,而是直接通过鼠类粪便和尿液污染人类的食物及生活用品,进而直接将病毒传播给人类。目前,该疫病的病毒宿主被认为是一种名叫多乳鼠(Mastomys)的鼠类。

▲拉沙热的病毒宿主被认为是一种名叫多乳鼠(Mastomys)的鼠类(图片来自网络)
作为一种传染性极强的国际性传染病,目前,拉沙热主要集中爆发于加纳、几内亚、利比里亚、塞拉利昂等西非国家,其中又以塞拉利昂和利比里亚最重。
据不完全数据统计,该疫病在西非地区每年感染人数约为10万-30万例。拉沙热的潜伏期非常长(6天 -1 个月),且早期症状非常难识别,其致死率虽然不高(1%),但死亡患者多集中于儿童,危重病例死亡率可达 15%,其中对孕妇的致死率高达 80%以上。值得注意的是,2018 年尼日利亚曾爆发过一起拉沙热疫病,此次疫情在一个月内导致超 300 人被确诊感染,其死亡率一度超过 20%。
“近亲”相残:灵长类
作为人类的“近亲”,黑猩猩、猴子这些灵长类动物也为人类送上了一位慢性杀手:人类免疫缺陷病毒(HIV),即艾滋病病毒。很长时间以来,人类盲目地相信大猩猩的血液能够强身壮阳,这种欲望激起他们举起屠刀、更加放肆地捕食大猩猩。然而讽刺的是,那些被人类视为“低人一等”的灵长类动物,选择使用一种特殊的慢性病毒开启了一场长达百年的报复。

▲白枕白眉猴被认为是HIV- 的天然宿主(图片来自网络)
与前文所讲的传染病不同,HIV 是一种感染人类免疫系统细胞的慢病毒,属逆转录病毒的一种,它并不会通过飞沫和正常的接触而传播,HIV感染者只有在发病后才被称之为艾滋病(AIDS)。
1920 年 HIV 在非洲出现,1981 年美国医疗机构首次确诊人类感染这一病毒。由于彼时里根政府并没有重视艾滋病的危险性,导致越来越多因血液传播而被感染的患者出现。颇为讽刺的是,在发现之初,欧美学者曾因病毒的命名及技术专利而“大打出手”,直至 1986 年才最终统一取名为“HIV”,以期更好地反映病毒导致免疫缺陷而不是致癌的这一性质。
根据 WHO 的数据统计,截至 2018 年全球共有 3790 万人被确诊感染,810万人甚至不知道自己已经感染HIV。仅2018年一年,因艾滋病死亡人数就达 77 万人,另有 170 万新增感染患者。最为可怕的是,这一数字还在不断增长,尤以撒哈拉及南非洲为重灾区,其次是南亚、东南亚,近年来东亚、东欧和中亚等地艾滋病涨幅呈现快速增长之势。
HIV 病毒可分为 HIV-1 和 HIV-2 两种。目前,人们普遍认为艾滋病主要是由 HIV-1 引起,而其天然宿主是来自喀麦隆南部的一种黑猩猩,这也是人类首次完全确定艾滋病毒毒株的所有源。
2018 年科学家证实,HIV-2 的天然宿主是一种生活在西非地区的白枕白眉猴。(撰文/记者 王雪莹 图文编辑 吉菁菁)
TIPS:
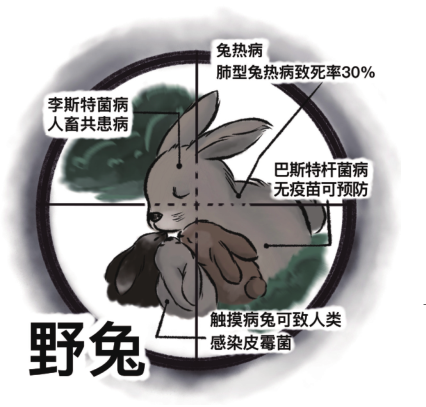
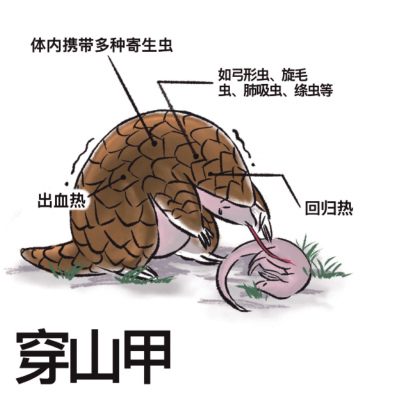
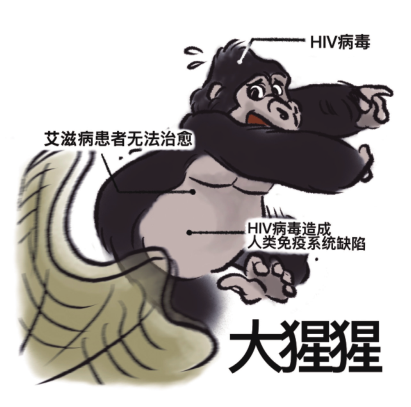
这些野生动物都“携毒”!
这些让人类心惊胆战的致命病毒,源头基本都来自于野生动物。
即使科技在今天发达如斯,食物链顶端的万物之灵长――人类也不能战胜所有,这些致命病毒或许要教会我们一件事―― 敬畏自然。


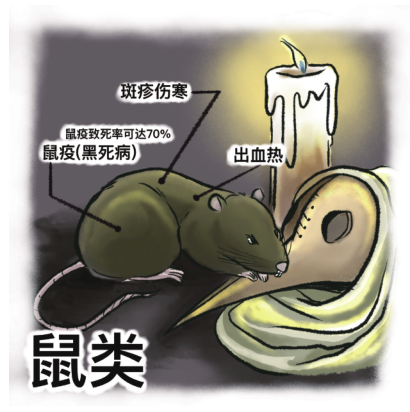

(绘图/记者 王雪莹)
审核专家:智利德萨罗洛大学流行病学及健康政策中心主任 Ximena Aguilera博士地址:长春市净月国家高新技术产业开发区永顺路1666号 邮编:130117 邮箱:ccostm@ccostm.com 电话:0431-81970000
技术支持:东北师范大学理想信息技术研究院
版权所有:长春中国光学科学技术馆 COPYRIGHT © WWW.CCOSTM.COM 吉ICP备15000181号-1

 本馆新闻
本馆新闻